问题:
今欲配制c(1/2H2S04)=1.0mol/L的标准溶液500mL,须用含96.0%(m/m)相对密度为1.84的浓硫酸多少毫升?
今欲配制c(1/2H2S04)=1.0mol/L的标准溶液500mL,须用含96.0%(m/m)相对密度为1.84的浓硫酸多少毫升?
已知M(H2S04)=98.08
则M(1/2H2S04)=49.04,
根据稀释前后溶质的物质的量不变的原则得到:
V(1/2H2S04)•c(1/2H2S04)=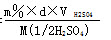
VH2S04=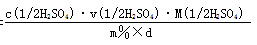 =
=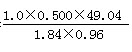 =13.9(mL)
=13.9(mL)
需要浓H2S0413.9mL
● 参考解析
本题暂无解析
相关内容
相关标签